[프레스나인] 일부 위탁사가 제조한 소화성궤양용제 ‘레바미피드’ 성분 제품들이 판매중지 행정처분을 받으면서 오리지널의약품을 비롯한 경쟁사 동일 성분 제네릭 품목이 수혜를 받고 있다.
레바미피드 성분은 오츠카제약 ‘무코스타’가 오리지널 제품이다. 위궤양과 급성위염, 만성위염의 급성악화기의 위점막병변(미란, 출혈, 발적, 부종) 개선에 사용하는 약물이다.
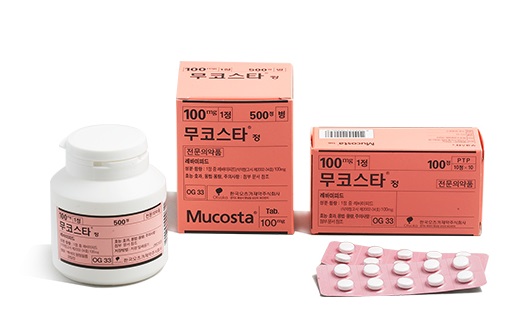
식품의약품안전처는 지난해 12월 비보존제약의 임의제조와 관련 ▲익수제약 ‘레바드미정’ ▲종근당 ‘레바라틴정’ ▲뉴젠팜 ‘레바미젠정’ ▲다산제약 ‘레바스코정100㎎’ ▲한국파비스제약 ‘레바피론정’ ▲대우제약 ‘레비스정’ ▲하나제약 ‘레스탐정’ ▲디에이치피코리아 ‘무코프로정’ ▲신풍제약 ‘무코피드정’ ▲비보존제약 ‘비보존레바미피드정100㎎’ ▲유앤생명과학 ‘레바미론정’ 등 총 11개 품목에 대해 회수·폐기 및 잠정 제조·판매 중지 처분을 내렸다.
이 11개 품목은 지난해 연간 76억원 원외처방액(유비스트 기준)을 기록했다. 이들 제품 중 하나제약 레스탐정(2월18일), 뉴젠팜 레바미젠정(4월5일), 신풍제약 무코피드정(4월11일), 종근당 레바라틴정(4월12일) 등 4개 제품만 급여가 재개된 상태다.
제네릭 제품들이 대거 행정처분을 맞으면서 무코스타는 지난 1~2월 2개월간 33억원 처방을 냈다. 전년동기 대비(30억원) 9.9% 증가한 금액이다. 같은 기간 유한양행 ‘레코미드’도 10억원으로 전년대비(2억원) 407.5% 증가, 대웅제약 ‘뮤코트라’도 7억원으로 전년대비(4억원) 70.9% 증가했다.
레바미피드 성분은 비보존제약에 이어 메디카코리아도 지난달 첨가제 임의사용과 제조기록서 거짓 작성 등 약사법 위반이 적발돼 행정처분 품목이 더 늘어났다. 해당 제품은 ▲메디카코리아 ‘메디카레바시드정’ ▲대원제약 ‘레바원정’ ▲동구바이오제약 ‘레미스타정’ ▲아이큐어 ‘레피드정’ ▲케이에스제약 ‘무코사정’ ▲한국신텍스제약 ‘레바엔티정100밀리그램’ 등 총 6개 품목이다.
이에 따라 무코스타를 비롯한 일부 제품들의 처방증가세도 계속될 것으로 예상되고 있다. 레바미피드는 보건복지부가 추진 중인 2023년 약제 급여 적정성 재평가 대상 성분이다. 재평가 기준은 ▲임상적 유용성 ▲비용 효과성 ▲사회적 요구도 등 기타 필요한 세부사항은 약제급여평가 위원회의 의견을 들어 정한다.
임상적 유용성은 임상진료지침·HTA보고서·임상연구문헌을, 비용 효과성은 대체 가능성 및 투약비용을, 사회적 요구도는 재정 영향·의료적 중대성 등을 고려해 평가한다.
오츠카제약 영업부 직원은 “무코스타는 임상논문 등 임상적 유용성에 대한 근거자료가 충분한 제품”이라며 “내부에서도 이번 급여 재평가와 관련해 별다른 우려를 하고 있지 않은 분위기”라고 전했다.