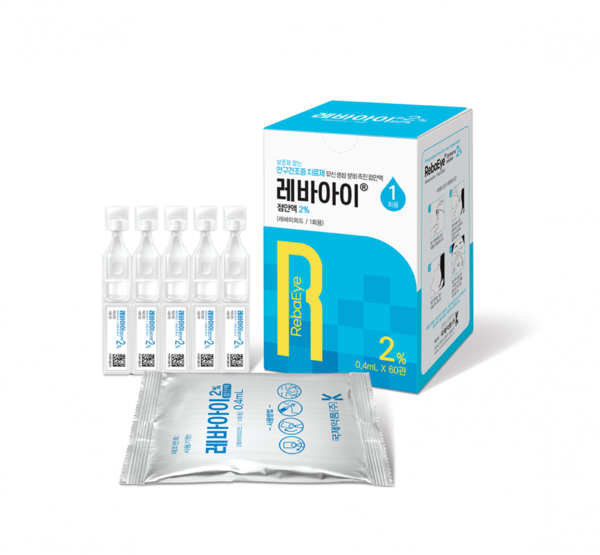
[프레스나인] 국제약품은 레바미피드 성분의 개량신약 ‘레바아이점안액2%’가 다회용에 이어 1회용 제품을 발매했다고 1일 밝혔다.
이번에 발매한 1회용 제품은 보존제로 인한 눈의 상피세포에 독성을 나타내지 않는 안전한 무보존제 점안제로 평가받고 있다. 1회용의 경우 기존 다회용의 15~30℃보다 넓은 온도 보관조건인 1~30℃에 따라 처방 환자의 의약품 보관이 좀 더 용이하다는 장점이 있다.
‘레바아이점안액2%(주성분 레바미피드)’는 국제약품이 세계에서 2번째로 허가 받은 제품으로 위점막, 장점막, 구강, 결막 등의 점막에서 분비되는 뮤신 분비를 촉진시켜 점막을 보호하는 기전을 가지고 있다.
일본 등에서는 현탁액으로 만들어져 이물감 및 자극성이 있었으나 국제약품이 이를 개선하는 기술을 적용해 개량신약으로 허가받았다. 임상에서도 기존 안구건조증 치료제보다 뛰어난 효과를 입증했다. 국내 안구건조증 환자 222명을 대상으로 레바미피드 2%(레바아이), 레바미피드 1%, 레바미피드 0%(위약군) 투여 후 유효성(각막 염색 점수(FCS) 변화, 결막 염색 점수(OSS) 변화, 무 마취 쉬르머검사, 눈물막 파괴 시간(TUBT), 안구표면질환지수)을 비교한 결과, 플루오레신 각막 염색 점수 변화량에서 레바아이가 4주, 8주, 12주차에 모두 위약군 대비 우월성을 확인했다.
1일 컴퓨터 사용시간이 4시간을 초과하는 안구건조증 환자들을 대상으로 레바아이(n=40) 또는 디쿠아포솔 3% 투여군(n=39)에 무작위 배정해 치료 전후 TUBT, 각결막 형광염색 등을 비교하는 임상을 진행한 결과, 플루오레신 각결막 염색 점수에서 2주, 4주, 8주째 모두 디쿠아포솔 대비 손상된 안구 상피에서 유의한 개선을 보였다.
눈물막 파괴 시간에서도 마찬가지였다. 레바아이는 2주, 4주, 8주차에 모두 기저치 대비 눈물막 안정성에 유의한 개선을 보인 반면 디쿠아포솔은 4주까지만 효과를 보였다. 해당 논문은 지난 8월3일 SCI급 저널인 BMC Ophthalmology 게재됐다.