'더 높은 효과, 더 오랜 지속성' 기대…CAR-T 대비 높은 살상능 확인
[프레스나인] 박셀바이오의 파이프라인 한 축을 NK 플랫폼이 차지하고 있다면, 다른 한 축은 CAR 치료제가 차지하고 있다고 할 수 있다.
CAR(Chimeric Antigen Receptor, 키메릭 항원 수용체) 치료제는 암세포 표면에 분포한 특정 단백질, 즉 항원을 인식하는 유전자를 T세포에 넣어 만든 항암면역 세포치료제다. CAR를 장착한 T세포(CAR-T)가 암세포에 선택적으로 반응해 결합한 뒤 독성물질 분비 등을 통해 제거한다.
CAR-T 치료제는 한 번의 투여로 암을 치료할 수 있어 큰 기대를 받고 있지만, 현재까지 FDA의 승인을 받은 CAR 치료제는 혈액암을 타겟으로 한 CAR-T 세포치료제 뿐으로, 전체 암의 95%를 차지하는 고형암을 대상으로 한 CAR 치료제는 없는 실정이다.
이에 업계에서는 고형암을 치료할 수 있는 CAR 치료제 개발에 박차를 가하고 있지만, 동일한 암에 대해 환자마다 다른 항원을 발현하는 '이형질성'과 끊임없이 변화해 T세포의 활동을 무력화하는 종양미세환경으로 인해 개발이 쉽지 않다. 여기에 FDA의 허가를 받은 CAR-T 치료제는 사이토카인 폭풍 등의 부작용과 치료제 내성이 한계로 지적되고 있다.
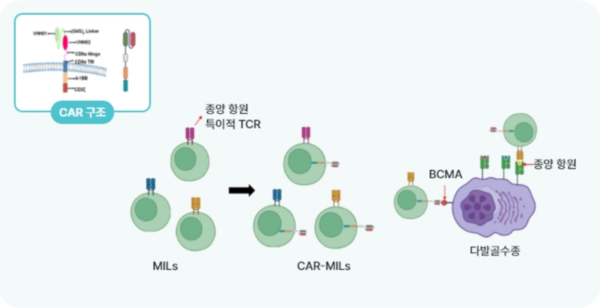
박셀바이오는 이러한 한계를 극복한 새로운 CAR 치료제 개발에 나선 것으로, 가장 먼저 골수침윤림프구(Marrow Infiltrating Lymphocytes, MIL)를 이용한 CAR-MIL 치료제 VCB-1201이 있다.
MIL은 골수에서 추출된 림프구를 이용해 제조한다. 일반적으로 CAR-T 세포치료제에 이용되는 말초혈액에서 분리되는 림프구와 달리 골수 미세환경의 독특한 면역학적 특성으로 인해 중앙 기억 T세포(Central Memory T Cell)가 풍부해 더 높은 항암효과와 더 오랜 지속성을 보인다는 특징이 있다.
VCB-1201는 이를 활용해 개발 중인 파이프라인으로, 다발골수종의 대표 항원인 BCMA(B-Cell Maturation Antigen)를 표적으로 한다. 다수의 종양 항원에 대한 중앙 기억 T세포가 풍부한 MIL에 CAR를 형질도입해, 특정 종양항원(BCMA)에 대한 특이성과 공동자극 영역 및 신호전달 영역을 지니게 함으로써 암세포 살상력을 높인다.
또한 MIL의 특성상 CAR-T와 비교했을 때 골수 미세환경에 대한 적응도가 높고 독성은 낮으며 제조법이 용이해 생산 측면에서도 경쟁력이 있다.
박셀바이오는 In vitro 및 In vivo 실험에서 CAR-T 치료제보다 높은 암세포 살상능을 확인한 바 있으며, 현재 제조 공정 확립과 함께 임상시험계획(IND) 제출을 위한 GLP 수준의 비임상시험을 진행 중이다.